
前列腺素概述
2023-05-05 15:04:30 点击数:早在20世纪30年代人们就已发现,精液含有调节子宫收缩的物质,人们推测此物质来源于前列腺,因此命名为前列腺素(prostaglandin,PG)。前列腺素为体内分布广泛、作用复杂的含20个碳原子的多不饱和脂肪酸激素。一般认为,前列腺素主要以旁分泌和自分泌的方式在组织局部发挥作用,但有些前列腺素如血管内皮细胞合成的前列腺环素(prostacyclin,PGI 2 ),可以进入血液循环,以经典的内分泌方式发挥作用。
前列腺素和与其相关的前列腺环素、血栓素(thromboxanes,TX)、白三烯(leukotrienes,LT)和脂氧素(lipoxins,LP)都来源于细胞膜的磷脂,后者在磷脂酶A2的作用下释放出花生四烯酸(arachidonicacid)。花生四烯酸再在环氧合酶(cyclooxygenase,COX)的作用下转化为环内过氧化物(cyclicendoperoxides),后者在不同异构酶(isomerase)的作用下,可以转化为前列腺素、血栓素和前列腺环素。因此环内过氧化物为前列腺素、血栓素和前列腺环素的共同前体(图5-5)。花生四烯酸还可以在5-脂氧酶或15-脂氧酶的作用下转化为白三烯或脂氧素。环氧合酶又称前列腺素H合成酶(prostaglandinHsynthetase,PGHS),体内存在固有型(constitutive)和诱导型(inducible)两种环氧合酶,分别称为COX-1和COX-2,后者在体内存在感染时可以受到诱导,此诱导可被糖皮质激素所阻断。
前列腺素的结构类似发夹,含有一个由5个碳原子组成的环和2条由此环发出的碳链,碳原子的位置从碳链最末端的羧基碳原子开始计数(见图5-5)。根据环上取代基的不同,前列腺素存在PGA、PGB、PGC、PGD、PGE、PGF、PGJ系列。它们的合成都经过PGG和PGH两个中间化合物。在所有前列腺素系列当中,以PGA、PGE和PGF含量最高、作用最为重要。前列腺素命名中的下标阿拉伯数字1~3是指两条侧链中双键的数目,而下标中的希腊字母α、β则指取代基的立体方位,在戊环平面之上的集团为β位,戊环平面之下为α位。PGF 2α 在9、11、15位共有3个在戊环平面之下的羟基,两条侧链中有2个双键,与PGA和PGE相比,它的水溶性最强,最容易溶入磷酸缓冲液,因此称其为前列腺素F,F取自瑞士语磷酸盐的第一个字母。PGE 2 除了第9位为酮基外,其他结构与PGF 2α 相同,由于少了一个羟基,因此其水溶性次于PGF 2α ,而更易溶于乙醚等有机溶剂。因此称其为前列腺素E,E取自乙醚的英文第一个字母。与PGF 2α 和PGE 2 相比,PGA的水溶性最差,其结构中除了第9位的羧基变为酮基外,第11位也缺少羟基。
前列腺素代谢的第一步是在15-羟基前列腺素脱氢酶(15-hysroxyprostaglandindehydrogenase,PGDH)的作用下,第15位的羟基发生氧化反应,然后13~14位之间的双键发生氧化,随后发生一系列的β氧化反应,逐步降解。肺脏为前列腺素的主要代谢器官,经过第一步PGDH的作用后,前列腺素即已转化为无活性的代谢产物,因此PGDH的作用在前列腺素的代谢中是非常重要的。PGDH已经被克隆,它是分子量29kD的细胞质酶,由两个相同的亚基组成,其作用需要辅酶NAD + 的参与,主要分布于肺脏、肾脏、肝脏、胎盘和绒毛膜。PGB和PGD不受PGDH的作用。尽管PGI 2 为PGDH的底物,但由于PGI 2 被肺细胞摄取的很少,因此只被肺脏不完全降解。
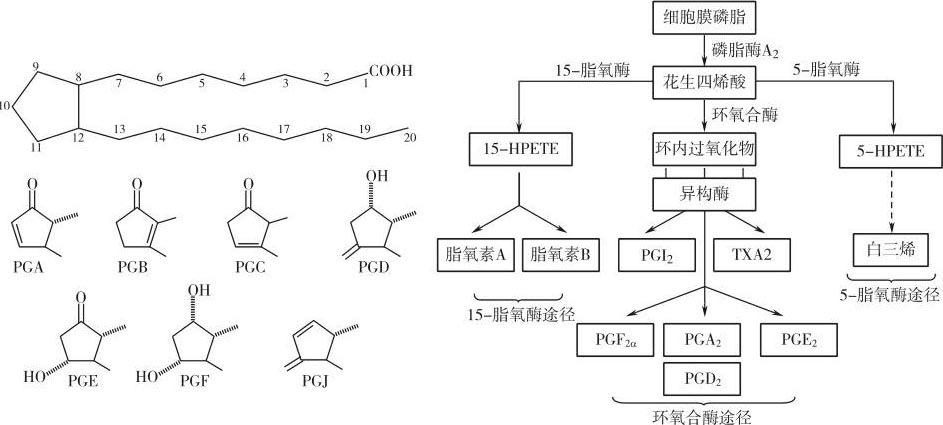
图5-5 前列腺素的结构和合成
前列腺素体内作用非常广泛。它通过作用于中枢神经系统的神经元如下丘脑、小脑和网状结构参与体温、自主神经和行为的调节;它作用于甲状腺、肾上腺、卵巢、睾丸等内分泌腺体影响这些腺体的激素分泌;它作用于胰腺和肠道黏膜影响这些组织的外分泌功能;它作用于生殖系统、心血管系统、消化系统和呼吸系统的平滑肌影响这些系统的功能;它还作用于血细胞影响免疫功能等。前列腺素的功能是通过细胞膜特异性的与G蛋白相耦联的受体所介导的,目前发现的PGE 2 受体至少存在EP1、EP2、EP3、EP4四型,EP1和EP3通过第二信使IP 3 /DAG动员钙离子和抑制cAMP的生成收缩平滑肌;EP2和EP4通过促进cAMP的生成舒张平滑肌。PGF 2α 的作用是通过FP受体由第二信使IP 3 /DAG所介导的。
越来越多的实验证据表明,胎盘、胎膜、蜕膜合成的前列腺素对妊娠过程中子宫/胎盘血流、胎儿肺功能、胎盘细胞分化、胚泡植入和分娩启动等重要功能起关键的调节作用,下面着重讨论前列腺素在胎盘/胎膜中的分布和功能。
1.妊娠期宫内组织前列腺素的分泌动物实验发现,羊早产时胎儿、母体和羊水的前列腺素水平均有升高,提示前列腺素可能参与分娩过程。人类实验发现,羊水前列腺素水平在分娩启动前稍有升高,分娩过程中继续显著升高。Rivanol引产时,羊水中花生四烯酸和PGF 2α 水平平行升高。人类观察结果进一步表明,宫内组织来源的前列腺素与分娩有关。宫内组织前列腺素测定结果显示,人类羊膜、绒毛膜、蜕膜、胎盘和子宫平滑肌都含有前列腺素,且以PGE 2 为主,但只有羊膜的前列腺素水平随分娩而升高。人类羊膜外植体灌流实验进一步证实,羊膜释放的前列腺素以PGE 2 为主,经过分娩过程的羊膜外植体、羊膜和蜕膜细胞释放较多的PGF 2α 和PGE 2 发现,羊膜具有转化花生四烯酸为前列腺素的能力,而且生成的前列腺素也以PGE 2 为主,提示羊膜存在合成前列腺素的酶系统。蜕膜以分泌PGF 2α 为主,子宫平滑肌则以分泌PGI 2 为主。
2.妊娠期宫内组织前列腺素合成酶的分布和活性
(1)PLA2:前列腺素合成的第一步是细胞膜的磷脂酸在PLA2的催化下,释放出前列腺素的前体花生四烯酸。花生四烯酸在细胞特异性氧化酶的作用下,再进一步沿着白三烯、脂氧素和前列腺素的代谢途径继续生成最终产物。人类胎膜、蜕膜存在PLA2的活性,其活性需要毫摩尔水平钙离子的存在,最适pH为8。妊娠晚期(38~41周)羊膜的PLA2活性比妊娠早期(13~17周)显著升高。PLA2存在两种同工异构酶,分别为由胰腺分离的一型PLA2和由关节腔液和血小板分离的二型PLA2。目前两型PLA2cDNA都已克隆,胎盘、羊膜、绒毛膜都含有二型PLA2mRNA,其中胎盘的含量较高。
磷脂酶C(PLC)的主要功能为促进细胞膜磷脂酰肌醇水解为第二信使二酰基甘油(DAG)和三磷酸肌醇(IP3)。近年来发现PLC也有促进细胞膜磷脂酸水解释放花生四烯酸的作用。人类羊膜、绒毛膜、蜕膜的PLC活性都很高,而且随孕期活性增高,妊娠晚期羊膜和包蜕膜PLC活性比妊娠早期分别增加了6倍和2倍。但有人比较了自然分娩和剖宫产羊膜和蜕膜的PLC活性,发现分娩过程中这些组织的PLC活性没有显著的改变。
(2)PGHS:前列腺素的合成不仅依赖于花生四烯酸的释放,还受前列腺素合成酶(PGHS)的调节。PGHS又称环氧合酶(cyclooxygenase,COX),它主要位于内质网、细胞核膜上,对花生四烯酸结合的米氏常数Km值为2~10μM。目前发现和克隆了两型PGHS,它们都为含血红素的蛋白,由2个70kD的亚基组成,既具有环氧酶的活性,又具有过氧化酶的活性,首先将花生四烯酸转化为含戊环的PGG2,然后进一步生成PGH2。PGH2在不同的异构酶的作用下沿不同的途径生成前列腺素、血栓素和前列腺环素。PGHS-1为细胞固有型(constitutive)酶,其表达不受其他激素的诱导,PGHS-1mRNA为2.7~3.0kb;PGHS-2为可诱导型(inducible)酶,可被PKC激活剂佛波醇酯、生长因子、细胞因子等所诱导,在多数细胞糖皮质激素抑制PGHS-2的表达,但在胎膜细胞糖皮质激素诱导其表达。PGHS-1和PGHS-2为不同基因的产物,其基因分别定位于9号染色体和1号染色体上,但两者结构之间仍有60%的同源性,PGHS-2的C末端含有一段17个氨基酸的特异性片段。一些非类固醇类抗感染药物如吲哚美辛(indomethacin)、阿司匹林等的作用机制就是对PGHS-2的抑制作用。此类药物还包括meclofenamicacid、niflumicacid、mefenamicacid、flufenamicacid、naproxen、phenylbutazone、ibuprofen。这些药物在高浓度时对磷酸二酯酶、氧化硫酸酶和胶原酶也有抑制作用。
妊娠晚期,胎膜的羊膜上皮、羊膜上皮下成纤维细胞、绒毛膜的滋养层细胞、蜕膜基质、血管和胎盘都表达PGHS-2mRNA及其蛋白。免疫组织化学染色显示PGE 2 及其代谢产物主要存在于胎盘的合体滋养层,少量存在于细胞滋养层。
胎膜PGHS的分布与糖皮质激素受体的分布类似,早产时这些组织的糖皮质激素受体水平升高,体外实验发现糖皮质激素促进羊膜PGHS-2mRNA的表达和酶的活性。这与糖皮质激素抑制其他组织PGHS的作用截然不同。糖皮质激素对胎膜前列腺素合成的促进作用与促分娩作用有关。糖皮质激素除了直接作用于PGHS促进前列腺素的合成外,还对宫内组织的CRH分泌具有正反馈作用,CRH也促进羊膜细胞PGE 2 的合成。因此,糖皮质激素可能还间接通过CRH促进前列腺素的合成分泌。其他调节人类胎膜组织前列腺素合成的因素包括细胞因子如IL-1、IL-4、IL-6、TNF等和生长因子如EGF、TGF等,它们促进胎膜前列腺素的合成和分泌,细胞因子的作用可能与感染导致的流产有关。
(3)PGDH:如上所述,前列腺素代谢的第一步是在PGDH的催化下,第15位的羟基发生氧化反应,然后13-14位之间的双键发生氧化,随后发生一系列的氧化反应,逐步降解。肺脏为前列腺素的主要代谢器官。胎膜的绒毛膜滋养层细胞表达大量的PGDH,PGDH阳性滋养层细胞占绒毛膜滋养层细胞60%~70%,但羊膜和蜕膜不表达PGDH。绒毛膜和胎盘组织都含有PGDH酶的活性,胎盘PGDH及其mRNA主要存在于合体滋养层和小叶外滋养层细胞。早产时绒毛膜PGDH的酶活性、蛋白和mRNA表达都有降低,感染导致早产时,绒毛膜PGDH的表达和酶的活性进一步降低。提示早产时,不仅存在前列腺素的合成增加,而且降解也减少。另外,自然分娩与剖宫产相比,前者绒毛膜的PGDH水平较低,提示前列腺素在早产和分娩启动机制中起着关键性的作用。
鉴于PGHS主要存在于羊膜,而PGDH主要存在于绒毛膜的事实,有人认为,正常妊娠时绒毛膜的PGDH起着降解羊膜来源的前列腺素作用,由此形成一道前列腺素到达子宫平滑肌的屏障。分娩或早产时绒毛膜的PGDH水平下降,使羊膜合成的前列腺素得以穿越绒毛膜作用于子宫平滑肌,收缩子宫、启动分娩。
关于PGDH的调节,目前所知不多。糖皮质激素除了促进羊膜PGHS的活性外,还抑制绒毛膜PGDH的活性,因此糖皮质激素既增源又节流,使前列腺素水平在宫内局部显著升高。炎症细胞分泌的细胞因子如IL-1、IL-6和TNF等对PGDH和PGHS的作用与糖皮质激素相似。
3.前列腺素在妊娠中的作用
(1)前列腺素与动物分娩:低等动物如羊的分娩是通过激活胎儿下丘脑-垂体-肾上腺轴启动的:妊娠晚期,胎儿血浆皮质醇水平升高,来自胎儿的皮质醇促进胎盘P450 C17 酶的活性,使孕酮向雌激素转化增加,导致孕激素水平的下降和雌激素水平的升高。与此同时,前列腺素(PGE 2 , PGF 2α )水平升高。胎儿给予糖皮质激素可以增加子宫和胎盘PGHS-2的活性。前列腺素可以通过旁分泌和自分泌的方式促进胎盘P450 C17 酶活性增加,使雌激素水平升高、孕激素水平下降。雌激素对子宫平滑肌与收缩有关的蛋白如connexin-43、催产素受体和前列腺素受体都有向上调节作用。另外,雌激素还可促进PGHS的活性,增加前列腺素的合成,使分娩中雌激素和前列腺素作用之间形成一正反馈环,加强子宫平滑肌的收缩。
(2)前列腺素与人类分娩:目前已有充分证据表明前列腺素在人类分娩过程中起着关键性的作用。妊娠期任何时间给予孕妇PGE 2 和PGF 2α 都可以导致流产。临床上经常将PGF 2α 与催产素联合羊膜腔内注射诱发早产、终止妊娠,PGE 2 与抗孕激素药物合用不仅可以加强前列腺素的诱发早产作用,而且可以减少PGE 2 的剂量,降低前列腺素对胃肠的副作用和子宫的疼痛。相反,前列腺素合成抑制剂则可以延长妊娠和治疗早产。虽然妊娠期母体血浆和羊水的前列腺素水平并未升高,但分娩期前列腺素的水平却有明显升高。有趣的是,分娩期血浆PGF 2α 代谢产物PGFM的增加幅度高于PGE 2 代谢产物PGEM,有人认为分娩时PGF 2α 的合成分泌增幅比PGE 2 为高或分泌的PGE 2 首先转化为PGF 2α ,后者再进一步代谢。
现已明确,分娩开始时羊水中花生四烯酸、PGE 2 、PGF 2α 、PGFM水平显著升高,而且变化时相与宫颈扩张相一致。注定需要催产素引产的孕妇,其羊水前列腺素的水平低下,提示前列腺素可能为分娩的前提条件。胎儿娩出后,羊水中前列腺素及其代谢产物的水平进一步增加,直到胎盘娩出。提示前列腺素还与胎盘的娩出有关。临床上有人根据前列腺素的这一特性用其治疗产后出血。
宫内组织前列腺素合成的重要特点就是羊膜为前列腺素PGE 2 合成的主要组织。自然分娩的羊膜组织PGE 2 的分泌率显著高于剖宫产,提示羊膜分泌的前列腺素与分泌有关。由于胎膜缺乏血管支配,羊膜前列腺素合成的条件可能受羊水成分的调节。实验表明,妊娠早期羊水对羊膜前列腺素的合成有抑制作用,而且强于分娩启动前羊水的抑制作用,分娩过程中羊水的抑制作用最弱。提示羊水中存在抑制前列腺素合成的物质,此物质随孕期和分娩的启动作用减弱。
人类羊膜、蜕膜和绒毛膜分别是妊娠期前列腺素PGE 2 、PGF 2α 和PGDH合成的主要组织。足月自然分娩的羊膜PGHS-2活性和mRNA水平均比剖宫产羊膜高,不明原因的早产和感染导致的早产羊膜PGHS-2活性及其mRNA水平都有显著升高,而绒毛膜PGDH水平则有下降,提示前列腺素参与了分娩过程。由于绒毛膜为宫内PGDH主要表达组织,又介于羊膜和蜕膜、子宫平滑肌之间,因此绒毛膜PGDH形成了一道前列腺素从羊膜侧向子宫侧转运的组织屏障,在妊娠期大部分时间,绒毛膜PGDH的活性比较高,可以有效地阻挡羊膜或绒毛膜合成的前列腺素对子宫的作用,妊娠晚期和分娩期由于胎膜PGHS水平的升高和PGDH的水平下降,使前列腺素显著升高。因此,设计PGHS抑制剂和PGDH刺激剂可为临床治疗早产提供有效治疗途径;而设计PGHS刺激剂和PGDH抑制剂或给予前列腺素可以终止妊娠、导致流产。
(3)前列腺素与子宫颈成熟:子宫颈的成熟包括软化、扩张和子宫颈管的消失为分娩过程必不可少的关键步骤之一,这一过程与前列腺素的作用有关。分娩时子宫颈PGE 2 和6-酮基-PGF 1a 的合成分泌增加,子宫颈成熟时也可在局部检测到高浓度的PGE 2 。PGE 2 为天然存在的前列腺素中最为有效的宫颈成熟促进剂。分娩开始后,子宫下段EP4受体表达显著增加。
(4)前列腺素基因敲除与胚泡植入的关系:敲除PGHS-2基因的纯合子小鼠,虽然炎症反应正常,但表现有肾脏异常的症状,肾脏的肾小球数目减少、肾小管萎缩和纤维化。此外还有排卵次数下降、胚泡植入障碍,因此生育能力下降。同样用药物抑制杂合子或正常动物PGHS-2酶的活性可以得到类似结果,胚泡植入受到抑制;抑制PGHS-1则不影响胚泡的植入过程。提示PGHS-2在排卵、胚泡植入和子宫内膜蜕膜化中起着关键性的作用。这与早期有关PGE2在子宫血管通透性和胚泡植入作用的观察结果相一致。
(5)前列腺素与脐带血管和主动脉导管闭锁:胚胎期间主动脉导管的开放有赖于循环和局部PGE 2 的水平,出生后动脉导管的关闭可能与氧分压的急剧变化有关。Nguyen等(1997)发现,胎鼠动脉导管平滑肌存在EP4受体,缺乏EP4受体的胎鼠,出生后动脉导管不能关闭,肺水肿、出血和瘀血,胎鼠不能成活。人类动脉导管闭锁不全的胎儿,血液PGE 2 、PGF和PGFM水平异常升高,其中尤为PGE 2 升高明显,它与动脉导管闭锁不全何为因果目前尚不清楚,很可能为动脉导管闭锁不全导致的PGE 2 代偿性增加。前列腺素对脐带血管出生后的闭锁可能起着类似的作用,脐带血管产生的前列腺素主要为PGE 2 和6-酮基-PGF 1α ,由于PGE 2 收缩血管,而前列腺环素舒张血管,因此脐带血管的舒缩和关闭很可能与局部PGE 2 和前列腺环素的比例有关。
